科研动态
近期来自北京大学基础医学院、北京大学国际癌症研究院的张宏权/战军研究团队在国际生物学顶刊eLife杂志上在线发表了题为“Loss function of tumor suppressor FRMD8 confers resistance to tamoxifen therapy via a dual mechanism”的研究论文,发现抑癌蛋白FRMD8通过调控ERα的水平抑制乳腺癌进程的新分子机制,有望成为克服他莫昔芬治疗耐药的潜在靶点。

乳腺癌严重威胁女性健康,其中超过70%的乳腺癌患者为ERα阳性乳腺癌。内分泌治疗是临床上针对ERα阳性乳腺癌常用的治疗方式,但仍有约40%患者存在原发性或继发性耐药,因此探究内分泌治疗耐药的新机制进而改善患者预后至关重要。FRMD8(含FERM结构域蛋白8)是一个新发现的含FERM结构域蛋白,张宏权教授领导的团队前期发现FRMD8是一个新的结直肠癌抑癌分子,通过调控细胞周期抑制结直肠癌进程(Cell Reports,2023)。然而,作为抑癌蛋白FRMD8在肿瘤中的生物学作用及其分子机制仍待深入挖掘。在这项新研究中,研究人员发现FRMD8在乳腺癌演进过程中也发挥重要的抑癌作用。FRMD8在转录和翻译后水平同时调控ERα的表达,进而抑制乳腺肿瘤对他莫昔芬治疗耐药。这项研究对阐明乳腺癌进展的分子机制和克服他莫昔芬治疗耐药具有重要的意义。
该团队利用基因修饰小鼠模型发现Frmd8的缺失加速了MMTV-PyMT小鼠乳腺肿瘤发生发展的进程,并使得MMTV-PyMT小鼠乳腺肿瘤对他莫昔芬治疗的耐药。单细胞转录组测序发现Frmd8的缺失导致小鼠乳腺激素敏感型(Hsd)上皮细胞减少,乳腺肿瘤细胞腔上皮特征丢失,ERα和PR表达下调。FRMD8的缺失可以通过下调FOXO3A表达进而抑制ESR1(ERα的编码基因)转录。同时,FRMD8与ERα相互作用,阻止UBE3A与ERα结合,进而抑制UBE3A介导的ERα经泛素-蛋白酶体途径降解的过程。最后,研究人员对多种乳腺癌细胞系中FRMD8的蛋白表达水平进行检测,发现随着细胞恶性程度的增加FRMD8表达降低,这种低表达是FRMD8基因启动子高甲基化的结果。采用DNA甲基转移酶的抑制剂可以重新启动FRMD8蛋白的表达水平,展示出靶向FRMD8基因启动子甲基化对乳腺癌他莫昔芬耐药的潜在治疗价值。作为乳腺癌进展的标志,FRMD8低表达预示着乳腺癌患者的不良预后。
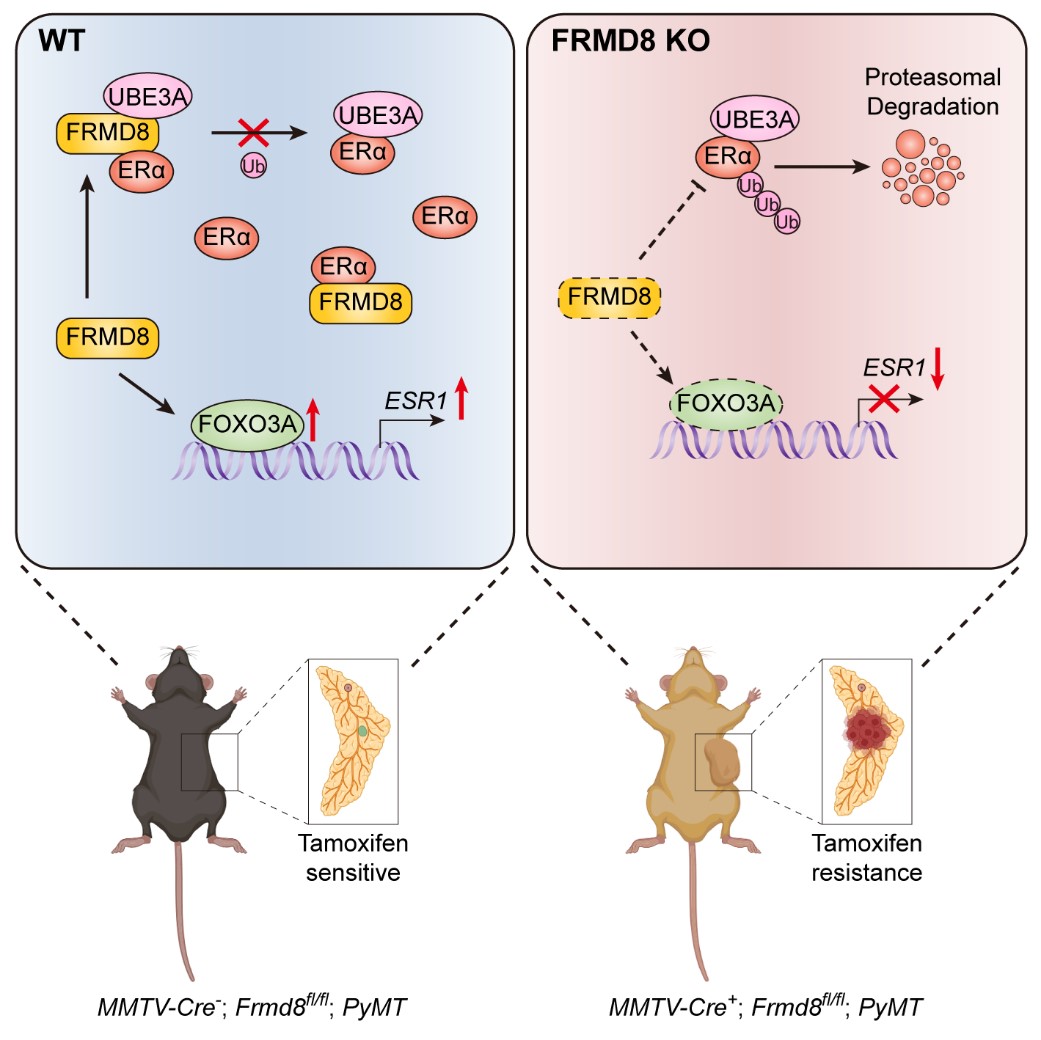
该研究揭示出FRMD8是一个新的乳腺癌抑癌分子,并且是一个潜在的乳腺癌预后标志物。FRMD8缺失在转录水平和翻译后水平通过双层机制下调ERα表达,提示FRMD8是一个潜在的他莫昔芬治疗预后预测的标志物,并有望成为逆转他莫昔芬治疗耐药的潜在靶点。
北京大学基础医学院博士研究生武威杰和博士后于淼为该论文的共同第一作者,北京大学基础医学院、北京大学国际癌症研究院张宏权教授和战军研究员、天津肿瘤医院乳腺中心郭晓静教授和军事医学研究院生物工程研究所徐小洁研究员为该论文的共同通讯作者。该研究受到科技部重点基础研究项目、国家自然科学基金重点、面上和青年科学基金项目、北大医学青年科技创新扬帆计划及中央高校基本科研业务费的资助。
论文链接:https://doi.org/10.7554/eLife.101888.1

