科研动态
磷元素作为构成生命的必需成分广泛参与膜磷脂、DNA/RNA等生物大分子的组成,并在能量传递和信号转导中发挥重要作用。无机磷酸盐(Inorganic phosphate, Pi)是细胞摄入磷的主要形式,其胞质内浓度需被严格调控以避免细胞毒性。XPR1作为目前已知唯一的哺乳动物磷酸盐向外转运蛋白,在维持细胞磷酸盐稳态中发挥关键作用。关于其调控机制,2020年的研究表明焦磷酸肌醇InsP8作为反映细胞内磷酸盐水平的信号分子,可通过与XPR1的SPX结构域结合促进其磷酸盐外排功能[1]。2022年的研究进一步揭示KIDINS220可与XPR1形成蛋白复合体,并调控XPR1的亚细胞定位及磷酸盐转运活性[2]。然而,这两种调控因子如何协同调控XPR1功能的分子机制,目前仍缺乏直接的结构生物学证据。

2025年3月24日,北大-清华生命科学联合中心、北京大学基础医学院尹玉新/梁令团队在Nature Communications杂志在线发表题为“Synergistic activation of the human phosphate exporter XPR1 by KIDINS220 and inositol pyrophosphate”的研究论文。该研究通过冷冻电镜技术解析了XPR1与KIDINS220锚蛋白重复结构域的复合物在多磷酸肌醇InsP6和底物磷酸盐存在或缺失条件下的多种构象,以及单独XPR1突变体在多磷酸肌醇InsP6和底物磷酸盐存在时的结构,揭示了焦磷酸肌醇InsP8与KIDINS220蛋白协同调控XPR1磷酸盐外排功能的分子机制。
研究团队首先通过AlphaFold2结构预测发现,KIDINS220蛋白的锚蛋白重复结构域(Ankyrin repeat domain,ARD)能够与XPR1蛋白C末端loop区的α螺旋结合。研究者随后共同表达XPR1-KIDINS220-ARD复合物并解析了该复合物在底物磷酸盐存在或缺失条件下的结构,二者呈现相似的跨膜结构域(TMD)同源二聚体结构。结构分析显示,这两种结构呈现磷酸根离子转运通道两侧闭合的关闭状态构象(称为XPR1C),且通道内部不含磷酸根离子的密度。
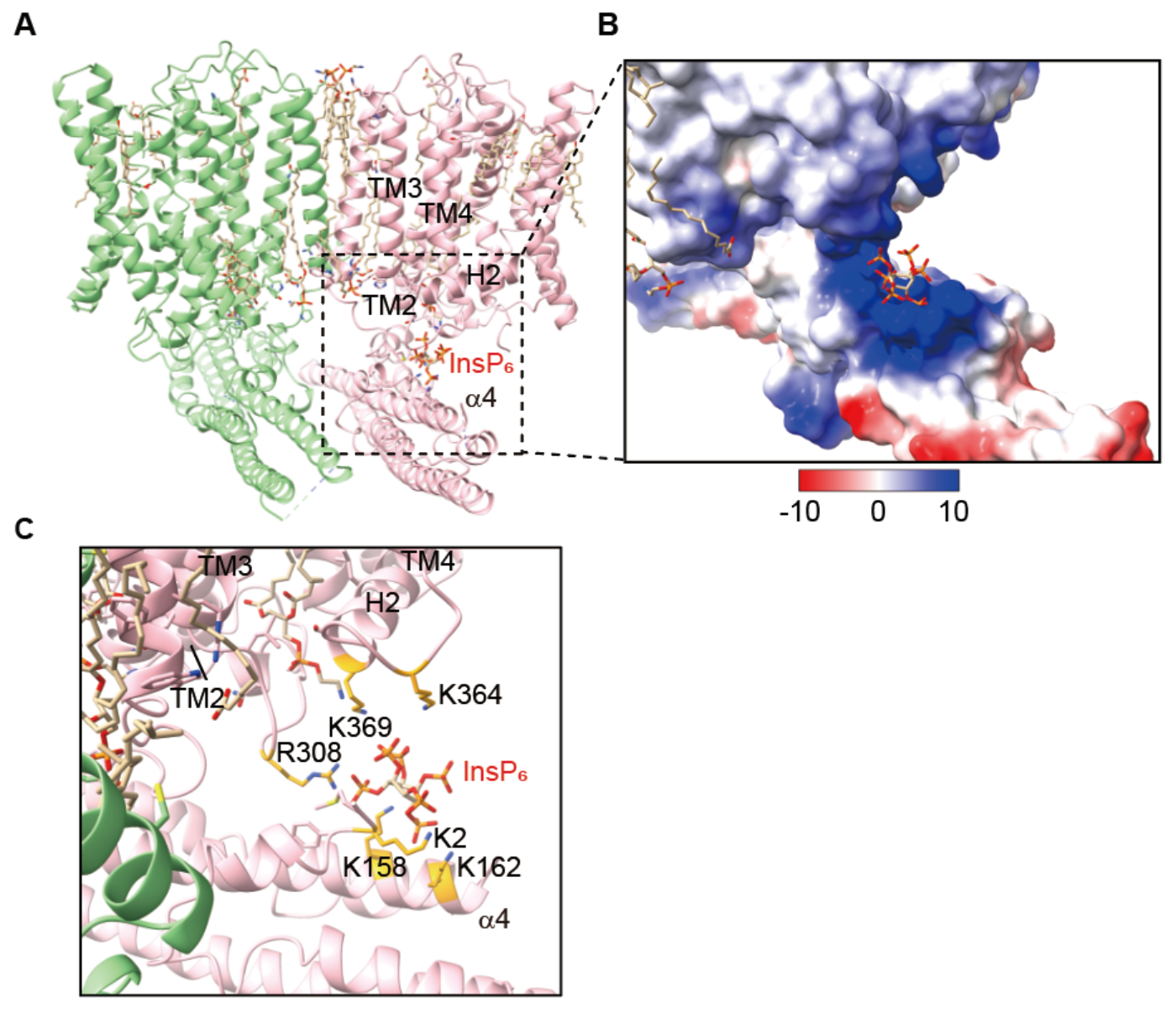
图1InsP6在SPX结构域和TMD间正电口袋结合示意图
研究者进一步探究多磷酸肌醇InsP6(焦磷酸肌醇InsP8的结构类似物)能否激活XPR1-KIDINS220-ARD复合物,并分别在磷酸盐存在与否条件下解析获得两种XPR1-KIDINS220-ARD-InsP6结构。在这两种结构中SPX结构域清晰可见(称为SPX结构域构象1),且InsP6均结合在由SPX结构域N端和TMD多个带正电荷氨基酸残基共同构成的正电口袋中(图1)。32P放射性同位素磷酸盐外排实验证明这些正电荷残基对XPR1的转运活性起重要作用。将InsP6替换为InsP8的分子动力学模拟显示,InsP8也可稳定结合于该口袋中。TMD的结构分析显示,底物磷酸盐不存在时,复合物保持关闭状态构象(称为XPR1C_SPX);而磷酸盐存在时,XPR1的九号跨膜螺旋(TM9)的胞外侧向外打开,形成开放的磷酸根离子转运通道,通道内可观察到多个磷酸根离子密度(称为XPR1OUT),提示该构象为活性状态。在XPR1OUT结构中,XPR1的C端结构域和KIDINS220的ARD结构域仍因高度动态性不可见。图1InsP6在SPX结构域和TMD间正电口袋结合示意图
研究者通过结构分析发现转运通道胞内侧的关闭主要由嵌入环(Glu622/Phe623基序)介导。功能实验证明E622A/F623A双点突变可显著增强XPR1的磷酸盐外排活性。进一步地对单独表达的XPR1-E622A/F623A突变体在底物和InsP6存在条件下的结构解析显示,该结构呈现TMD外侧闭合,但内侧通道打开的向内朝向状态的构象(称为XPR1IN),可观察到有磷酸根离子结合在胞内腔开口处。此结构中,InsP6转而结合在两个SPX结构域之间,且相比于构象1,SPX结构域整体翻转了约180°(称为SPX结构域构象2),可能是由于KIDINS220的ARD结构域位阻效应缺失的结果。此时,嵌入环后方的C端结构域部分序列与SPX结构域发生相互作用而被稳定。
研究者同时分析了磷酸根离子的转运通道,并从中鉴定了三个与Pi结合相关的关键区域,并利用功能实验验证这些重要氨基酸对XPR1磷酸盐外排活性的影响。从上述结构与功能实验结果出发,研究者提出了XPR1蛋白受KIDINS220和InsP8调控的磷酸根外排功能工作模型(图2):仅存在底物时XPR1与XPR1-KIDINS220复合物均处于无法介导磷酸盐转运的关闭状态;只存在InsP8时,XPR1跨膜结构域主要处于关闭状态,当嵌入环脱离胞内腔时,XPR1呈现向内朝向状态,此时磷酸根离子可进入转运通道中;而当InsP8和KIDINS220同时存在时,SPX结构域发生翻转,InsP8转而结合在TMD和SPX结构域之间,此时KIDINS220通过锚蛋白结构域结合XPR1 C端loop的α螺旋,通过自身摆动持续为嵌入环脱离胞内腔提供动力,进而促进磷酸根离子转运冲破外腔,表现为向外开放状态构象。
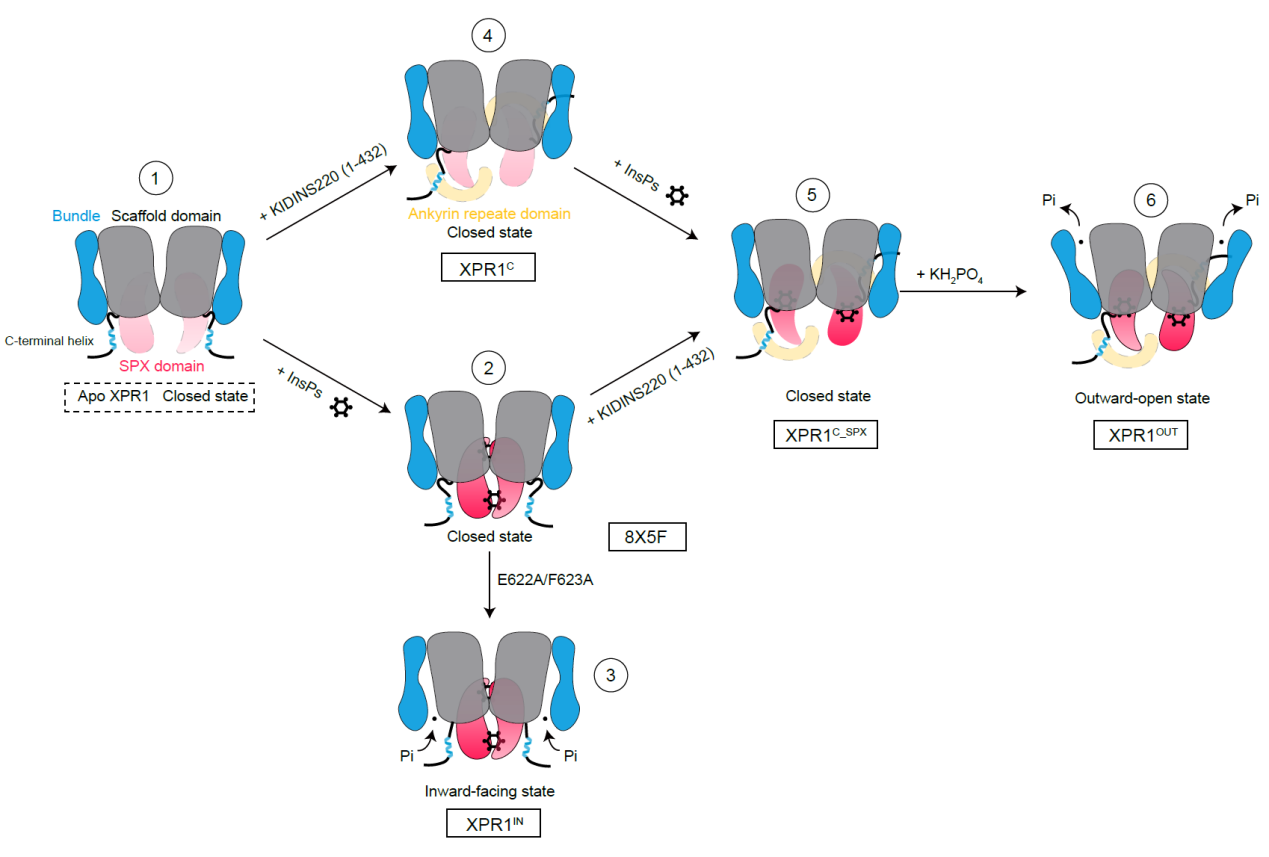
图2 XPR1受KIDINS220和InsP8调控的工作模型
相较于前期发表的XPR1冷冻电镜结构研究文章[3-7],该研究进一步探讨了KIDINS220对XPR1构象及磷酸盐转运功能的调控作用,并鉴定了新的多磷酸肌醇/焦磷酸肌醇结合位点,为阐明XPR1的磷酸盐外排机制提供了新视角。
北京大学基础医学院、北大-清华生命科学联合中心尹玉新教授和北京大学基础医学院梁令副研究员为本论文的共同通讯作者。北京大学基础医学院博士研究生佐鹏为本论文的唯一第一作者。
原文链接:https://www.nature.com/articles/s41467-025-58200-y

