学院新闻
赵颖课题组发现自噬在肿瘤微环境中促进胰腺癌增殖的新机制
胰腺导管腺癌(PDAC)以广泛的纤维性结缔组织增生为特征,其中癌症相关成纤维细胞(CAFs)是肿瘤微环境中最关键的基质细胞之一。多项研究表明,癌症相关成纤维细胞与肿瘤的增殖、转移和化疗耐药密切相关。
自噬是一种溶酶体依赖性蛋白质降解过程,在肿瘤微环境中具有重要作用。自噬可以通过多种方式作用于癌症相关成纤维细胞,并使其促进肿瘤生长。然而,自噬在癌症相关成纤维细胞中的具体作用机制还需要进一步的探索。
2022年7月11日,北京大学基础医学院赵颖教授团队在Autophagy杂志上在线发表了题为 “Autophagy loss impedes cancer-associated fibroblast activation via downregulating proline biosynthesis” 的研究论文,发现了癌症相关成纤维细胞中的自噬缺陷通过抑制脯氨酸生物合成和胶原蛋白生成来阻碍癌症相关成纤维细胞的激活。(北京大学基础医学院博士研究生白婧如和北京大学第三医院刘彤副教授为本文的共同第一作者。北京大学医学部基础医学院赵颖教授为通讯作者。)
2022年8月 18日,北京大学基础医学院赵颖教授团队、清华大学胡泽平教授团队联合复旦大学附属华山医院傅德良教授团队在Nature Cancer杂志上在线发表了题为 “Cancer associated fibroblasts employ NUFIP1-dependent autophagy to secrete nucleosides and support pancreatic tumor growth “ 的研究论文,阐述了癌症相关成纤维细胞通过NUFIP1依赖的自噬途径,在胰腺癌肿瘤微环境中分泌核苷,促进胰腺癌增殖的新机制。(北京大学基础医学院博士研究生原梦、美国华盛顿弗雷德·哈钦森癌症研究中心涂博博士、复旦大学附属华山医院李恒超医生以及清华大学药学院博士后庞欢欢为本文的共同第一作者。北京大学医学部基础医学院赵颖教授,清华大学药学院胡泽平教授和复旦大学附属华山医院傅德良教授为共同通讯作者。)
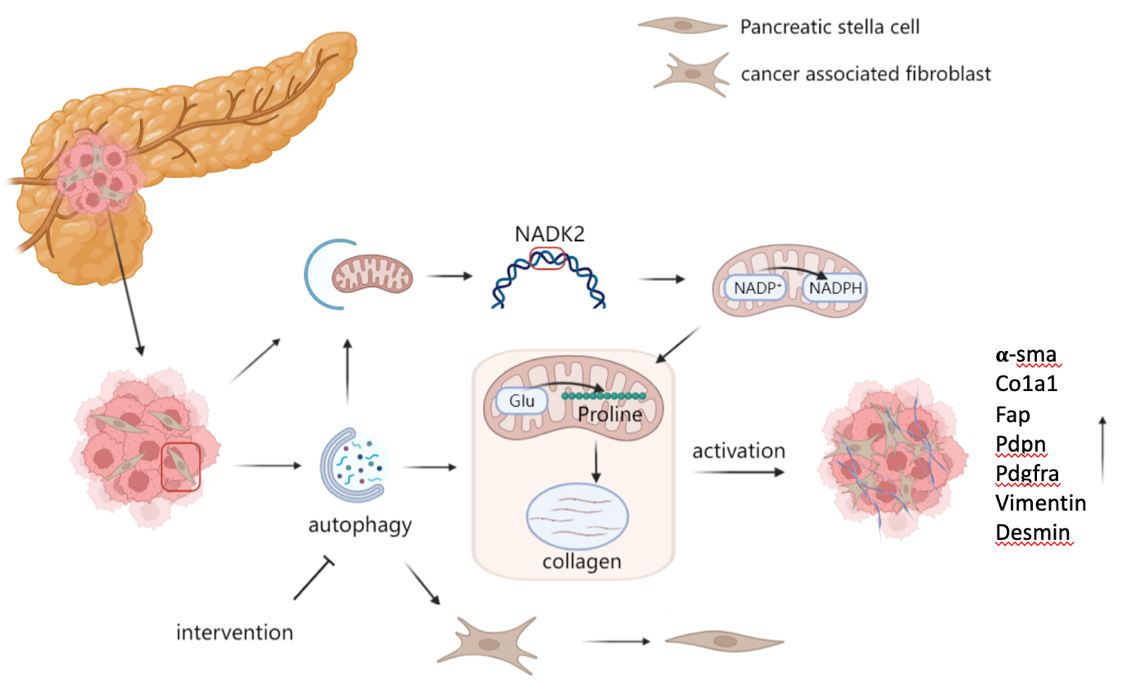
CAFs是与胰腺导管腺癌 (PDAC) 相互作用并促进肿瘤生长、转移和治疗抵抗的最关键的基质细胞之一。该课题组发现自噬通过调节脯氨酸生物合成影响CAFs活化,并且,研究表明CAFs通过线粒体自噬调控NADK2的表达,调节线粒体NADPH的产生,进而影响脯氨酸生物合成。此外,在野生型与线粒体自噬相关基因Prkn全身敲除小鼠中构建胰腺原位肿瘤模型,发现线粒体自噬缺陷小鼠中肿瘤重量减轻,进一步证实了CAF的线粒体自噬在PDAC进展中的重要性。因此,抑制CAFs线粒体自噬可能为以基质为靶点的抗癌干预治疗提供新的策略。

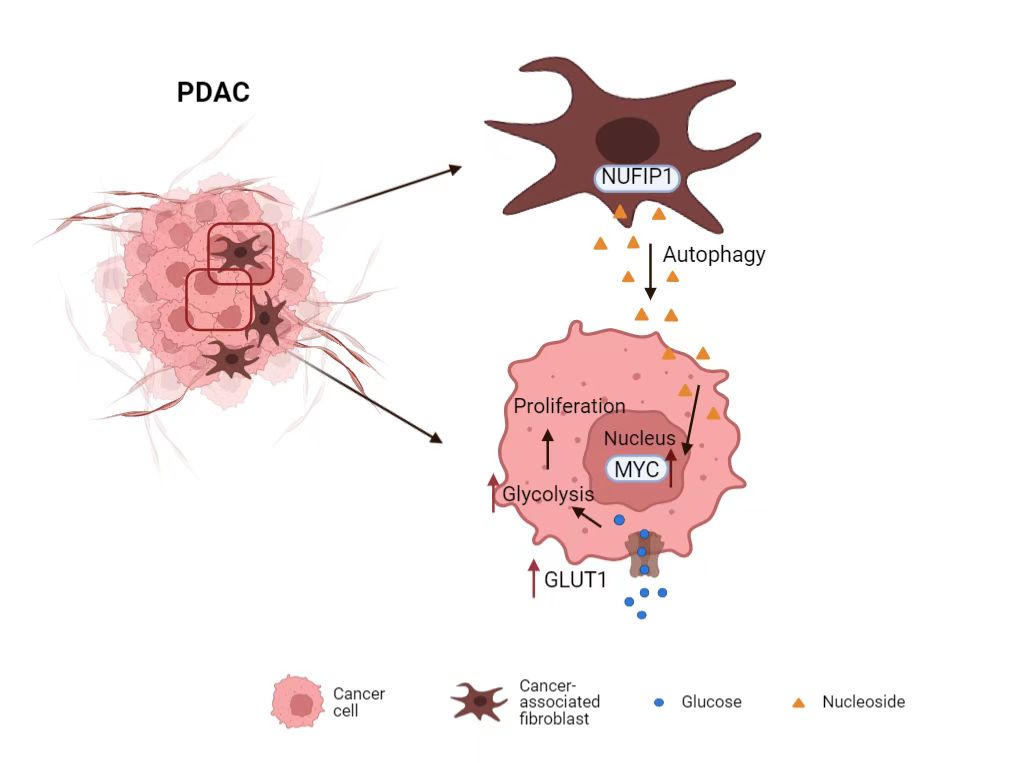
该团队又进一步发现NUFIP1依赖性自噬在CAFs促进PDAC的生长中具有关键作用。 NUFIP1可以通过调控核糖体RNA的降解释放核苷,但是并未观察到核糖体蛋白的降解。进一步研究发现, 敲除NUFIP1能够抑制CAFs中的核糖体RNA降解,并抑制其分泌核苷,而这会直接影响在谷氨酰胺剥夺下的肿瘤细胞的增殖。
有趣的是,核苷作为一种营养物质,并未直接被肿瘤细胞利用,而是通过MYC诱导肿瘤细胞对葡萄糖的消耗。GSEA富集分析发现,在谷氨酰胺缺乏的情况下,CAFs能够上调PDAC细胞中 “MYC targets” 类别基因的表达。进一步实验发现,CAFs分泌的核苷能够上调肿瘤细胞内MYC蛋白的水平。MYC是调控葡萄糖代谢的重要转录因子,MYC水平的上调,提高了肿瘤细胞对葡萄糖的摄取和利用,缓解了肿瘤细胞在肿瘤微环境中所面对的营养压力。 因此,CAFs通过NUFIP1依赖性自噬分泌的核苷提高了PDAC对于葡萄糖的利用,进一步促进了PDAC的增殖和生长。

以上工作得到了科技部重点研发计划、国家自然科学基金面上项目,北京大学临床+X专项资助。
原文链接:
https://www.tandfonline.com/doi/full/10.1080/15548627.2022.2093026
https://doi.org/10.1038/s43018-022-00426-6
(北京大学基础医学院)

