学院新闻
Blood|孙金鹏/铁璐团队揭示β-arrestin的N-同型半胱氨酸化系统性地重塑血小板中GPCR偏好性信号转导
2025年2月12日,北京大学基础医学院孙金鹏教授团队与铁璐教授团队,在Blood发表“N-homocysteinylation of β-arrestins biases GPCR signaling and promotes platelet activation”。首次揭示HHcy通过N-同型半胱氨酸化β-arrestin重塑GPCR信号偏好性,系统性阐明HHcy促血栓形成的分子机制,并提出靶向GPCR偏好性信号通路的抗血栓治疗新策略。该研究建立的“病理修饰-信号偏好性重塑”模型,不仅适用于血栓性疾病,也为GPCR信号偏好性相关的神经退行性疾病、代谢综合征等提供了共性机制框架。

高同型半胱氨酸血症(HHcy)是动脉粥样硬化、冠心病、脑卒中等血栓性疾病的独立危险因素。血小板作为凝血系统的核心执行者,其过度活化是血栓形成的“导火索”。临床数据显示,HHcy患者血小板对ADP、凝血酶等G蛋白偶联受体(GPCRs)激动剂的反应性显著增强,但分子机制尚不清楚。GPCRs作为血小板活化的核心调控者(如PAR1/4、TP、P2Y1/P2Y12受体),其信号失衡如何被HHcy“劫持”是领域内亟待解决的科学问题。
研究团队以血小板为突破口,结合临床样本分析、基因编辑小鼠模型及质谱技术,首次揭示HHcy通过N-同型半胱氨酸化修饰β-arrestin1/2,重塑血小板PAR1/4、TP、P2Y1/P2Y12等GPCR信号网络的动态平衡的分子机制:
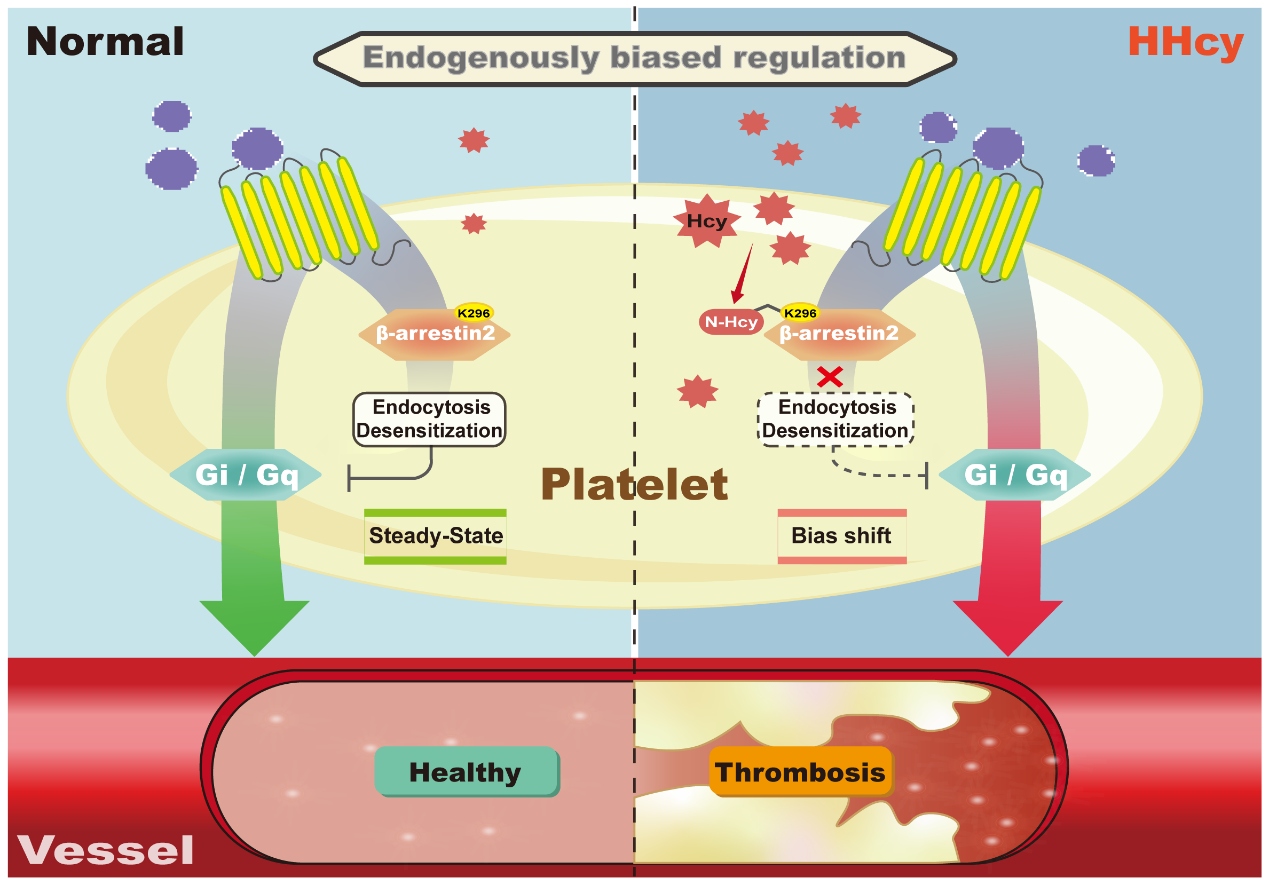
病理修饰靶点锁定——利用特异性探针AT-3与高分辨率液相色谱-串联质谱技术,团队在β-arrestin2的赖氨酸残基K296处发现特异性N-Hcy修饰信号,提示此为病理修饰的关键位点。
信号偏好性转换——K296位点的N-同型半胱氨酸化显著抑制β-arrestin2介导的GPCR内化与G蛋白信号脱敏,导致下游Gi/Gq信号通路持续性偏好激活,从而放大血小板对ADP、凝血酶等激动剂的响应,加速血栓形成。
基因编辑验证机制——通过CRISPR-Cas9技术构建β-arrestin2 K296R敲入小鼠,团队证实该突变可逆转HHcy对血小板活化的促进作用,且显著延缓动脉血栓形成,明确K296位点是HHcy致病的关键分子开关。
此外,传统观点认为HHcy通过氧化应激或炎症通路间接影响心血管系统,而本研究发现,HHcy环境下,依赖β-arrestin信号通路的抗炎药物(如GPR120激动剂DHA)疗效显著降低,而偏向激活Gs蛋白通路的TGR5激动剂INT-777仍能有效抑制炎症。这提示G蛋白偏好性激动剂可能是HHcy患者的更优治疗选择,为个性化药物设计指明方向。
综上所述,该研究建立的“病理修饰-信号偏好性重塑”模型,不仅适用于血栓性疾病,也为GPCR信号偏好性相关的神经退行性疾病、代谢综合征等提供了共性机制框架。
北京大学基础医学院孙金鹏教授与铁璐副教授为本文共同通讯作者。北京大学基础医学院章琳琪博士、硕士研究生车长晓,以及杜亚琴博士为本文共同第一作者。该研究得到了北京大学王宪教授、周德敏教授、王初教授、北京大学第三医院张龙主任医师以及复旦大学赵世民教授的许多帮助与支持。
原文链接:

